Nembutal solución oral
$1,200.00
Nembutal solución oral Dosis de Lathal para Eutanasia
Fenobarbital Solución Oral Descripción
Los barbitúricos son depresores no selectivos del sistema nervioso central (SNC) que se utilizan principalmente como sedantes-hipnóticos. En dosis subhipnóticas, también se utilizan como anticonvulsivos. Los barbitúricos y sus sales de sodio están sujetos a control en virtud de la Ley Federal de Sustancias Controladas. El fenobarbital es un derivado del ácido barbitúrico y se presenta en forma de pequeños cristales o polvo cristalino, blancos e inodoros, muy poco solubles en agua; solubles en alcohol, éter y soluciones de hidróxidos alcalinos y carbonatos fijos; y poco solubles en cloroformo. El fenobarbital es ácido 5-etil-5-fenilbarbitúrico y tiene la fórmula empírica C 12H 12N 2O 3. Su peso molecular es 232,24. Su fórmula estructural es la siguiente El pentobarbital en solución oral (PB) es un fármaco eutanásico en dosis de 2 a 10 gramos, que causa la muerte en 15-30 minutos. Informamos de un caso de recuperación de autoenvenenamiento deliberado letal con pentobarbital con concentraciones séricas de fármaco confirmatorias.
Informe de un caso
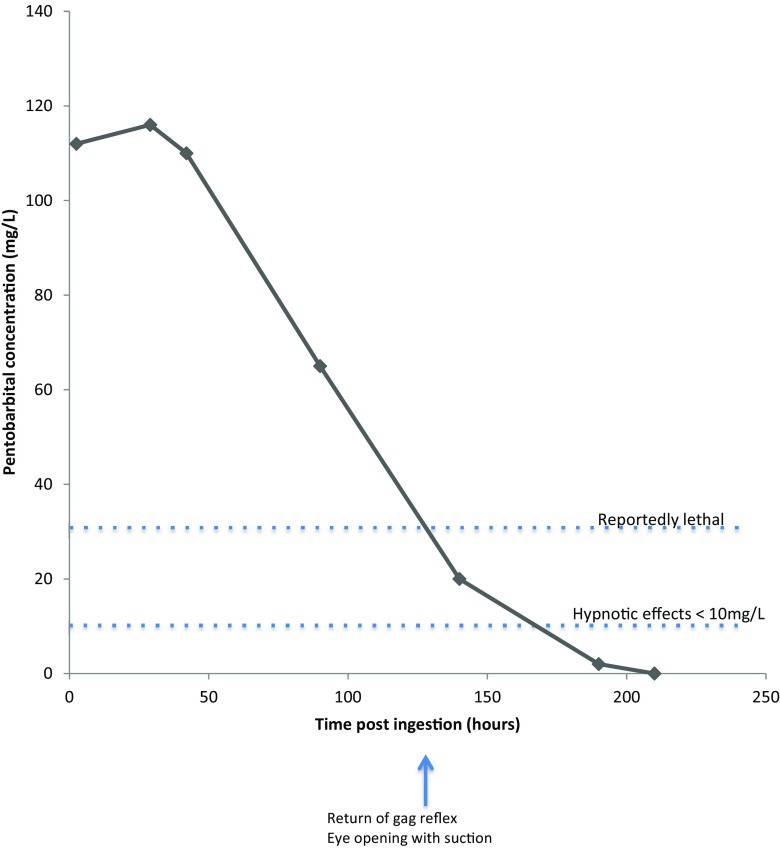
Un varón de 45 años compró 20 gramos de polvo PB por Internet. Ingirió este polvo y alertó a su madre 10 minutos después. Ella lo encontró inconsciente y comenzó la reanimación cardiopulmonar (RCP). A los 20 minutos de la ingestión, llegaron los servicios médicos de urgencias e iniciaron el soporte vital avanzado. A su llegada al servicio de urgencias, su frecuencia cardiaca era de 116 lpm, su presión arterial de 117/62 mmHg y estaba recibiendo una infusión de epinefrina. Estaba hipotónico e hipotérmico, con ausencia de reflejos del tronco encefálico. El ECG y el TAC cerebral eran normales. Se le administró carbón activado y fue ingresado en la UCI. Permaneció en coma con ausencia de reflejos del tronco encefálico hasta el día 5. El angiograma cerebral del día 3 fue normal. En el análisis cualitativo de orina se detectó pentobarbital, lo que sugería que la causa del coma eran los efectos continuados del fármaco. Fue extubado el día 10, recuperándose por completo. A las 2,5 horas de la ingestión, la concentración de PB era de 112 mg/L; la PB alcanzó un máximo de 116 mg/L a las 29 horas; la PB era de 2 mg/L a las 190 horas e indetectable a las 200 horas de la ingestión.
Debate
Se ha informado de que la concentración media de PB en las víctimas mortales es de unos 30 mg/L. Este paciente sobrevivió a concentraciones séricas más elevadas con reanimación cardiopulmonar precoz y soporte cardiorrespiratorio prolongado en la UCI. La evaluación de la muerte cerebral debe aplazarse hasta que se haya eliminado adecuadamente la PB.
El pentobarbital (Nembutal) es un sedante-hipnótico barbitúrico de acción corta que se utiliza ampliamente en la práctica veterinaria para la anestesia y la eutanasia. También se recomienda como fármaco para la eutanasia o el suicidio asistido debido a su rápida aparición del coma y a la percepción de una muerte tranquila. Estas informaciones populares en los medios de comunicación de que el pentobarbital es un método pacífico de suicidio han provocado un mayor interés por obtenerlo en jurisdicciones donde está menos regulado [1]. Es poco probable que se adopten medidas de reanimación en estas circunstancias.
Informamos de un caso de supervivencia tras un autoenvenenamiento deliberado con un fármaco potencialmente dosis letal de pentobarbital obtenido a través de Internet, en un paciente que se arrepintió de sus actos y buscó ayuda casi inmediatamente. Se presentan concentraciones séricas seriadas confirmatorias del fármaco en el contexto de la evolución clínica del paciente.
Historia de un caso
Un varón de 45 años ingirió impulsivamente 20 gramos de pentobarbital (Nembutal) que había comprado por Internet a una fuente en el extranjero 2 años antes. Tenía antecedentes de trastorno afectivo bipolar, neuralgia del trigémino y dolor crónico. Tomaba regularmente venlafaxina, gabapentina y asenapina. Alertó a su madre 10 minutos después de tomar la sobredosis. Ella contactó inmediatamente con los servicios médicos de urgencias (SEM). Cuando regresó junto a él, estaba en el suelo e inconsciente, y ella comenzó inmediatamente la reanimación cardiopulmonar (RCP). Los SEM llegaron 10 minutos después de la llamada (aproximadamente 20 minutos después de la ingestión) y lo encontraron en parada cardiaca con actividad eléctrica sin pulso. Continuó la reanimación cardiopulmonar y se iniciaron medidas de soporte vital avanzado (SVA). Recibió dos dosis intravenosas de 1 mg de epinefrina durante la reanimación inicial, y el retorno de la circulación espontánea (ROSC) se produjo al cabo de 10 min. El paciente fue intubado y ventilado. 30 minutos más tarde sufrió una nueva parada cardiaca breve, que se resolvió tras otros 2 minutos de reanimación cardiopulmonar y 1 mg más de epinefrina. Se le inició una infusión de epinefrina a 100 μg/min, se le administró un bolo de 500 ml de solución salina normal y se le trasladó al servicio de urgencias (SU).
El paciente llegó a urgencias 95 minutos después de la llamada inicial al SEM. En el momento de la presentación, estaba inconsciente (Glasgow 3/15) sin sedación adicional, tenía las pupilas dilatadas y fijas, y estaba apnéico con el ventilador y sin reflejos en el tronco encefálico. Estaba hipotérmico (33,8 °C). La frecuencia cardiaca era de 116 lpm, y la PA de 117/62 mmHg con una infusión de epinefrina a 100μg/min. La gasometría venosa mostró pH 7,02, pCO2 60 mmHg, HCO3 15 mmol/L, y 11,9 mmol/L de lactato. El etanol, el paracetamol y el salicilato séricos eran indetectables. El ECG fue normal y la TC cerebral no reveló ninguna anomalía aguda. Se administró una dosis única de 50 g de carbón activado por sonda nasogástrica y fue ingresado en la UCI.
Se decidió tratamiento de soporte y no instaurar ninguna técnica de eliminación extracorpórea. El día 1 en la UCI desarrolló poliuria, con una diuresis máxima de 300 ml/h, e hipernatremia (Na sérico 149 mmol/L), por lo que se le trató con una dosis de desmopresina.
Requirió apoyo vasopresor con infusión de norepinefrina (dosis máxima de 30 μg/min) durante los primeros 5 días de su ingreso. Permaneció en coma sin sedación, con ausencia de reflejos del tronco encefálico, lo que suscitó discusiones en torno al diagnóstico de muerte cerebral. El tercer día se realizó una angiografía cerebral de cuatro vasos. El resultado fue una perfusión cerebral normal. La orina enviada para análisis cualitativo por cromatografía de gases-espectrometría de masas (GC-MS) detectó pentobarbital, confirmando los efectos continuos de la droga como la causa probable del coma persistente. El día 5, se produjo un retorno del reflejo nauseoso a la succión y la apertura de los ojos a estímulos dolorosos. Se inició una infusión de propofol para permitir la tolerancia al tubo endotraqueal a partir del día 7. Sin embargo, la extubación se retrasó hasta el día 8. Sin embargo, la extubación se retrasó debido al desarrollo de neumonitis por aspiración. Finalmente fue extubado el día 10 tras la sobredosis y fue dado de alta al día siguiente. Necesitó 10 días más de hospitalización para seguir con el tratamiento de la neumonitis por aspiración y fisioterapia de reacondicionamiento. Se recuperó completamente desde el punto de vista neurológico y confirmó la ingestión de 20 gramos de pentobarbital en polvo mezclado con agua. Fue dado de alta a un centro de salud mental el día 22 tras la sobredosis. Permaneció ingresado allí 3 semanas más antes de ser dado de alta, con seguimiento psiquiátrico ambulatorio.
Las concentraciones séricas seriadas de pentobarbital se analizaron retrospectivamente mediante cromatografía líquida de alta resolución/espectrometría de masas (HPLC/MS) y se resumen en la Fig. 1. La concentración máxima fue de 116 mg/mL aproximadamente 29 horas después de la ingestión (terapéutica 1,8-4,7 mg/L).
Fig. 1.
Se obtuvo el consentimiento por escrito para la publicación de este caso y se facilitó a la revista.
Fenobarbital Solución Oral - Farmacología Clínica
Los barbitúricos son capaces de producir todos los niveles de alteración del estado de ánimo del SNC, desde excitación hasta sedación leve, hipnosis y coma profundo. La sobredosis puede producir la muerte. En dosis terapéuticas suficientemente altas, los barbitúricos inducen la anestesia.
Los barbitúricos deprimen la corteza sensorial, disminuyen la actividad motora, alteran la función cerebelosa y producen somnolencia, sedación e hipnosis.
El sueño inducido por barbitúricos difiere del sueño fisiológico. Los estudios de laboratorio del sueño han demostrado que los barbitúricos reducen la cantidad de tiempo que se pasa en la fase de movimientos oculares rápidos (MOR) del sueño o la etapa de soñar. Además, en las fases III y IV, el sueño disminuye. Tras la interrupción brusca de los barbitúricos utilizados regularmente, los pacientes pueden experimentar un marcado aumento de los sueños, pesadillas y/o insomnio. Por lo tanto, se ha recomendado la retirada de una dosis terapéutica única durante 5 ó 6 días para disminuir el rebote REM y la alteración del sueño que contribuyen al síndrome de abstinencia del fármaco (por ejemplo, la dosis debe disminuirse de 3 a 2 dosis/día durante 1 semana).
En los estudios, se ha observado que el secobarbital sódico y el pentobarbital sódico pierden la mayor parte de su eficacia para inducir y mantener el sueño al cabo de 2 semanas de administración continuada del fármaco, incluso con el uso de dosis múltiples. Al igual que ocurre con el secobarbital sódico y el pentobarbital sódico, cabe esperar que otros barbitúricos (incluido el amobarbital) pierdan su eficacia para inducir y mantener el sueño al cabo de unas 2 semanas. Los barbitúricos de acción corta, intermedia y, en menor medida, prolongada se han prescrito ampliamente para tratar el insomnio. Aunque en la literatura clínica abundan las afirmaciones de que los barbitúricos de acción corta son superiores para producir el sueño, mientras que los compuestos de acción intermedia son más eficaces para mantenerlo, los estudios controlados no han logrado demostrar estos efectos diferenciales. Por lo tanto, como medicamentos para dormir, los barbitúricos tienen un valor limitado más allá de su uso a corto plazo.
Los barbitúricos tienen escasa acción analgésica a dosis subanestésicas. Más bien, en dosis subanestésicas, estos fármacos pueden aumentar la reacción a estímulos dolorosos. Todos los barbitúricos presentan actividad anticonvulsiva en dosis anestésicas. Sin embargo, de los fármacos de esta clase, sólo el fenobarbital, el mefobarbital y el metarbital son eficaces como anticonvulsivantes orales en dosis subhipnóticas.
Los barbitúricos son depresores respiratorios, y el grado de depresión respiratoria depende de la dosis. Con dosis hipnóticas, la depresión respiratoria producida por los barbitúricos es similar a la que se produce durante el sueño fisiológico y se acompaña de una ligera disminución de la presión arterial y la frecuencia cardíaca.
Los estudios en animales de laboratorio han demostrado que los barbitúricos provocan reducciones del tono y la contractilidad del útero, los uréteres y la vejiga urinaria. Sin embargo, las concentraciones de los fármacos necesarias para producir este efecto en humanos no se alcanzan con dosis sedantes/hipnóticas.
Los barbitúricos no alteran la función hepática normal, pero se ha demostrado que inducen enzimas microsomales hepáticas, aumentando y/o alterando así el metabolismo de los barbitúricos y otros fármacos (ver Interacciones medicamentosas en el apartado PRECAUCIONES).
FARMACOCINÉTICA
Los barbitúricos se absorben en diversos grados tras su administración oral o parenteral. Las sales se absorben más rápidamente que los ácidos. La tasa de absorción aumenta si la sal de sodio se ingiere como solución diluida o se toma con el estómago vacío.
La duración de la acción, que está relacionada con la velocidad a la que los barbitúricos se redistribuyen por el organismo, varía entre las personas y en la misma persona de vez en cuando.
El fenobarbital se clasifica como barbitúrico de acción prolongada cuando se administra por vía oral. Su inicio de acción es de 1 hora o más, y su duración de acción oscila entre 10 y 12 horas.
Los barbitúricos son ácidos débiles que se absorben y distribuyen rápidamente a todos los tejidos y fluidos, con altas concentraciones en el cerebro, el hígado y los riñones. La solubilidad lipídica de los barbitúricos es el factor dominante en su distribución en el organismo. Cuanto más soluble en lípidos sea el barbitúrico, más rápidamente penetrará en todos los tejidos del organismo. Los barbitúricos se unen a las proteínas plasmáticas y tisulares en grado variable, y el grado de unión aumenta directamente en función de la solubilidad lipídica.
El fenobarbital tiene la menor solubilidad en lípidos, la menor unión plasmática, la menor unión a proteínas cerebrales, el mayor retraso en el inicio de la actividad y la mayor duración de la acción. La semivida plasmática del fenobarbital en adultos oscila entre 53 y 118 horas, con una media de 79 horas. La semivida plasmática del fenobarbital en niños y recién nacidos (menos de 48 horas) oscila entre 60 y 180 horas, con una media de 110 horas.
Los barbitúricos se metabolizan principalmente por el sistema enzimático microsomal hepático, y los productos metabólicos se excretan en la orina y, con menor frecuencia, en las heces. Aproximadamente de 25% a 50% de una dosis de fenobarbital se elimina sin cambios en la orina. La excreción de barbitúricos no metabolizados es una característica que distingue a los de acción prolongada de los pertenecientes a otras categorías, que se metabolizan casi en su totalidad. Los metabolitos inactivos de los barbitúricos se excretan como conjugados del ácido glucurónico.
Indicaciones y uso de Nembutal solución oral
A. Sedante
B. Anticonvulsivante - Para el tratamiento de convulsiones generalizadas y parciales.
Contraindicaciones
El fenobarbital está contraindicado en pacientes hipersensibles a los barbitúricos, en pacientes con antecedentes de porfiria manifiesta o latente y en pacientes con alteración marcada de la función hepática o enfermedad respiratoria en la que sea evidente disnea u obstrucción.
Advertencias
1. Formación de hábitos
El fenobarbital puede crear hábito. Puede producirse tolerancia y dependencia psicológica y física con el uso continuado (ver ABUSO DE DROGAS Y DEPENDENCIA y Farmacocinética bajo FARMACOLOGÍA CLÍNICA). Los pacientes que tienen dependencia psicológica de los barbitúricos pueden aumentar la dosis o disminuir el intervalo de dosificación sin consultar a un médico y, posteriormente, pueden desarrollar una dependencia física de los barbitúricos. Para minimizar la posibilidad de sobredosis o el desarrollo de dependencia, la prescripción y dispensación de barbitúricos hipnótico-sedantes debe limitarse a la cantidad necesaria para el intervalo hasta la siguiente cita. La interrupción brusca después de un uso prolongado en una persona dependiente del fármaco puede provocar síntomas de abstinencia, incluyendo delirio, convulsiones y posiblemente la muerte. Los barbitúricos deben retirarse gradualmente de cualquier paciente que se sepa que está tomando dosis excesivas durante largos períodos de tiempo (ver ABUSO Y DEPENDENCIA DE DROGAS).
2. Dolor agudo o crónico
Debe tenerse precaución cuando se administran barbitúricos a pacientes con dolor agudo o crónico, ya que podría inducirse una excitación paradójica o enmascarar síntomas importantes. Sin embargo, el uso de barbitúricos como sedantes en el postoperatorio quirúrgico y como coadyuvantes de la quimioterapia del cáncer está bien establecido.
3. Uso en el embarazo
Los barbitúricos pueden causar daños fetales cuando se administran a una mujer embarazada. Estudios retrospectivos de casos controlados han sugerido una conexión entre el consumo materno de barbitúricos y una incidencia de anomalías fetales superior a la esperada. Los barbitúricos atraviesan fácilmente la barrera placentaria y se distribuyen por los tejidos fetales; las concentraciones más elevadas se encuentran en la placenta, el hígado fetal y el cerebro. Los niveles en sangre fetal se aproximan a los niveles en sangre materna tras la administración parenteral.
Se producen síntomas de abstinencia en bebés nacidos de mujeres que reciben barbitúricos a lo largo del último trimestre del embarazo (ver ABUSO Y DEPENDENCIA DE DROGAS).
Si Fenobarbital se utiliza durante el embarazo o si la paciente se queda embarazada mientras toma este medicamento, la paciente debe ser informada del peligro potencial para el feto.
4. Uso en niños
Se ha informado de que el fenobarbital se asocia a déficits cognitivos en niños que lo toman para convulsiones febriles complicadas.
5. Efectos sinérgicos
Precaución
Los barbitúricos pueden crear hábito. Puede producirse tolerancia y dependencia psicológica y física con el uso continuado (ver ABUSO Y DEPENDENCIA DE DROGAS).
Los barbitúricos deben administrarse con precaución, si acaso, a pacientes con depresión mental, tendencias suicidas o antecedentes de abuso de drogas.
Los pacientes ancianos o debilitados pueden reaccionar a los barbitúricos con marcada excitación, depresión o confusión. En algunas personas, especialmente niños, los barbitúricos producen repetidamente excitación en lugar de depresión.
En pacientes con daño hepático, los barbitúricos deben administrarse con precaución e inicialmente en dosis reducidas. Los barbitúricos no deben administrarse a pacientes que presenten signos premonitorios de coma hepático.
Los efectos sistémicos de los corticosteroides exógenos y endógenos pueden verse disminuidos por el Fenobarbital. Por lo tanto, este producto debe administrarse con precaución a pacientes con función hipoadrenal limítrofe, independientemente de si es de origen hipofisario o suprarrenal primario.
Información para pacientes
La siguiente información e instrucciones deben darse a los pacientes que reciben barbitúricos.
1. El uso de barbitúricos conlleva un riesgo asociado de dependencia psicológica y/o física. Debe advertirse al paciente que no aumente la dosis del fármaco sin consultar a un médico.
2. Los barbitúricos pueden alterar las capacidades mentales y/o físicas necesarias para la realización de tareas potencialmente peligrosas, como conducir un automóvil o manejar maquinaria. Los pacientes deben ser advertidos en consecuencia.
3. No debe consumirse alcohol mientras se toman barbitúricos. El uso simultáneo de barbitúricos con otros depresores del SNC (p. ej., alcohol, narcóticos, tranquilizantes y antihistamínicos) puede producir efectos depresores del SNC adicionales.
Referencias
- 1.Cantrell FL, Nordt S, McIntyre I, Schneir A. Death on the doortep of a border community-intentional self-poisoning with veterinary pentobarbital. Clin Toxicol. 2010;48:849-850. doi: 10.3109/15563650.2010.512562. [DOI] [PubMed] [Google Académico]
- 2.Bosshard G, Ulrich E, Bar W. 748 casos de suicidio asistido por una organización suiza de derecho a morir. Swiss Med Wkly. 2003;133:310-317. doi: 10.4414/smw.2003.10212. [DOI] [PubMed] [Google Académico]
- 3.Mactier R, Laliberte M, Mardini J, Ghannoum M, Lavergne V, et al. Tratamiento extracorpóreo de la intoxicación por barbitúricos: recomendaciones del grupo de trabajo EXTRIP. Am J Kidney Dis. 2014;64:347-358. doi: 10.1053/j.ajkd.2014.04.031. [DOI] [PubMed] [Google Académico]
- 4.Roberts DM, Buckley NA. Enhanced elimination in acute barbiturate poisoning-a systematic review. Clin Toxicol. 2011;49:2-12. doi: 10.3109/15563650.2010.550582. [DOI] [PubMed] [Google Académico]
- 5.Heinemeyer G, Roots I, Dernhardt R. Monitoring of pentobarbital plasma levels in critical care patients suffering from increased intracranial pressure. Ther Drug Monit. 1986;8:145-150. doi: 10.1097/00007691-198606000-00003. [DOI] [PubMed] [Google Académico]
- 6.McCarron MM, Schulze BW, Walberg CB, Thompson GA, Ansari A. Sobredosis de barbitúricos de acción corta. Correlation of intoxication score with serum barbiturate concentration. JAMA. 1982;248:55-61. doi: 10.1001/jama.1982.03330010029026. [DOI] [PubMed] [Google Académico]
- 7.Sullivan R, Hodgman MJ, Kao L, Tormoehlen LM. Baclofen overdose mimicking brain death. Clin Toxicol. 2012;50:141-144. doi: 10.3109/15563650.2011.654209. [DOI] [PubMed] [Google Académico]
- 8.Neavyn MJ, Stolbach A, Greer DM, Nelson LS, Smith SW, et al. ACMT position statement: determining brain death in adults after drug overdose. J Med Toxicol. 2017;13:271-273. doi: 10.1007/s13181-017-0606-8. [DOI] [Artículo libre PMC] [PubMed] [Google Académico]
Sé el primero en valorar “Nembutal oral solution” Cancelar respuesta
Productos relacionados
Nembutal
Nembutal










Valoraciones
No hay valoraciones aún.